HGH176-191 (Humanes Wachstumshormonfragment 176-191) ist ein C-terminales Fragment des menschlichen Wachstumshormons (HGH), das aus 15 Aminosäuren besteht (Sequenzposition 176-191). Als modifizierte Form von HGH behält es die Regulation des Fettstoffwechsels des natürlichen HGH bei, umgeht jedoch die wachstumsfördernden Eigenschaften von HGH und damit verbundene Nebenwirkungen (z. B. Insulinresistenz oder Organhypertrophie). Dieses Fragment hat große Aufmerksamkeit in den Bereichen Fettleibigkeitsmanagement, Sportmedizin und Anti-Aging erregt, da es darauf abzielt, Lipolyse (Lipolylyse) zu fördern und die Adipogenese (Liposynthese) zu hemmen.
Was ist HGH176-191?
HGH176-191 bezeichnet ein spezifisches Segment des menschlichen Wachstumshormonmoleküls, das sich von der Aminosäure 176 bis zur Aminosäure 191 erstreckt. Diese spezifische Aminosäuresequenz verleiht ihr einzigartige biologische Eigenschaften. Chemisch ist es ein lineares Polypeptid, das aus 16 Aminosäuren besteht, die durch spezifische Peptidbindungen verbunden sind. Die verschiedenen Seitenketten der Aminosäuren bestimmen ihre chemischen Eigenschaften und räumliche Konformation, was wiederum ihre Wechselwirkungen mit anderen Biomolekülen im Körper beeinflusst.
HGH176-191 Struktur
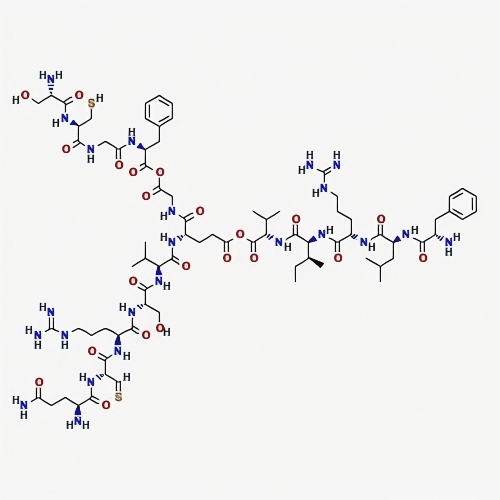
HGH176-191 Forschung
Auswirkungen des Wachstumshormons auf den Glukosestoffwechsel
Wachstumshormon verringert die Insulinsensitivität. Ein Aspekt davon ist, dass Wachstumshormon die Lipolyse stimuliert und eine erhöhte Freisetzung freier Fettsäuren ermöglicht. Wenn freie Fettsäuren zahlreicher werden, hemmen sie die Aufnahme und Nutzung von Glukose durch Muskelgewebe und stören gleichzeitig die Insulinsignalwege, was wiederum die Insulinsensitivität verringert. So gibt es beispielsweise bei Patienten mit Akromegalie eine Überproduktion von Wachstumshormon, und es tritt häufig eine Insulinresistenz auf, die sich als erhöhter Blutzucker, aber nicht als niedrige Insulinspiegel äußert, was darauf hindeutet, dass die glukosesenkende Wirkung von Insulin gehemmt wird, was eng mit der Wirkung des Wachstumshormons auf die Insulinsensitivität zusammenhängt. Ein weiterer Aspekt ist, dass Wachstumshormon auch die Expression einiger entzündlicher Faktoren erhöht, wie zum Beispiel des Tumornekrosefaktor-Alpha (TNF-α), die den Insulinsignalweg weiter stören, die Insulinresistenz verschlimmern und den Glukosestoffwechsel beeinflussen [1].
Wachstumshormon fördert die hepatische Gluconeogenese. Glykolyse bezeichnet den Prozess, bei dem zuckerfreie Substanzen wie gluconeogene Aminosäuren und Glycerol in der Leber in Glukose umgewandelt werden. Wachstumshormon induziert eine Erhöhung der Expression wichtiger Enzyme der Glukoneogenese wie Phosphoenolpyruvatcarboxykinase (PEPCK) und Glukose-6-phosphatase, was den Prozess der Glukoneogenese beschleunigt und zu einer erhöhten Glukoseproduktion aus der Leber führt und den Blutzuckerspiegel ansteigen lässt. Unter physiologischen Bedingungen trägt diese Regulation dazu bei, die Stabilität des Blutzuckers aufrechtzuerhalten, und wenn der Körper unter Stress oder Hunger steht, liefert das Wachstumshormon Energie, indem es die Glukoneogenese fördert. Wenn jedoch eine abnormale Erhöhung der Wachstumshormonsekretion auftritt, kann eine übermäßige Glukoneogenese zu einer anhaltenden Erhöhung des Blutzuckers führen, was eine Störung des Glukosestoffwechsels auslöst [1] .
Die Regulation des Fettstoffwechsels durch das Wachstumshormon wirkt sich auch indirekt auf den Glukosestoffwechsel aus. Wie bereits erwähnt, fördert Wachstumshormon die Lipolylyse, und die freigesetzten freien Fettsäuren können als Rohstoffe für die hepatische Glukoneogenese dienen und die Glukoseaufnahme in den Muskeln beeinflussen, was die Glukoneogenese weiter fördert. Gleichzeitig kann Glycerol aus Lipolylyse auch in den Glukoneogenen-Weg gelangen und als Substrat für die Glukoneogenese dienen. Außerdem beeinflusst das Wachstumshormon die Differenzierung und Funktion der Adipozyten, reguliert die Fettspeicherung und -mobilisation und beeinflusst damit das Gleichgewicht zwischen Energiestoffwechsel und Glukoneogenese [1].
Wachstumshormon spielt auch eine Rolle bei der Funktion der Bauchspeicheldrüseninsel β-Zellen. Unter normalen Bedingungen können moderate Mengen an Wachstumshormon helfen, die Insel- β-Zellfunktion und die Insulinsekretion aufrechtzuerhalten. Langanhaltende hohe Wachstumshormonspiegel können jedoch negative Auswirkungen auf die Zellen der Bauchspeicheldrüseninsel β haben. Eine Möglichkeit ist, dass durch Wachstumshormon induzierte Insulinresistenz dazu führen kann, dass die Zellen der Pankreasinsel β chronisch mit übermäßiger Insulinsekretion überlastet werden, was im Laufe der Zeit zu einer beeinträchtigten β-Zellfunktion der Insel und der relativen Insulinsekretion führen kann, was die Glukosestoffwechselstörungen weiter verschlimmert. Ein weiteres Beispiel ist, dass Wachstumshormon die Synthese, Verarbeitung und Sekretion von Insulin beeinträchtigen kann, indem es den Signaltransduktionsweg in den β-Zellen der Bauchspeicheldrüseninsel beeinflusst und so die normale Regulierung des Blutzuckers beeinträchtigt [1].
Auswirkungen auf den Lipidstoffwechsel
Obwohl es keine Studien gibt, die sich direkt mit den langfristigen Auswirkungen von HGH176-191 auf den Lipidstoffwechsel befassen, können Studien zur Wachstumshormontherapie einige Referenzen liefern. In einer Wachstumshormon-Behandlungsstudie mit japanischen Kindern jünger als dem Gestationsalter (SGA) bis zu 260 Wochen wurden während der Behandlung günstige Veränderungen der Lipidprofile festgestellt, die während des gesamten Studienzeitraums erhalten blieben. Daher wird vermutet, dass HGH176-191 als Fragment des Wachstumshormons den Lipidstoffwechsel, wie etwa die Regulierung des Cholesterinspiegels, unter langfristiger Wirkung positiv beeinflussen kann. Cholesterin ist ein wichtiger Bestandteil von Lipiden, darunter Gesamtcholesterin, Low-Density-Lipoprotein-Cholesterin (LDL-C) und High-Density-Lipoprotein-Cholesterin (HDL-C). LDL-C wird oft als "schlechtes Cholesterin" bezeichnet, und seine Erhöhung wird mit einem erhöhten Risiko für Herz-Kreislauf-Erkrankungen in Verbindung gebracht; während HDL-C als "gutes Cholesterin" bekannt ist, das anti-atherosklerotische Effekte hat. HGH176-191 kann das Verhältnis dieser Cholesterinwerte durch einen Mechanismus regulieren, um die lipidmetabolische Homöostase aufrechtzuerhalten, was wiederum das Risiko für Herz-Kreislauf-Erkrankungen senkt [2].
Auswirkungen auf Körperzusammensetzung und Energiestoffwechsel
KÖRPERZUSAMMENSETZUNG: Die Auswirkungen von HGH176-191 lassen sich aus Studien zu den Auswirkungen von Wachstumshormon auf die Körperzusammensetzung ableiten. Die Behandlung mit Wachstumshormonen bei Kindern mit SGA führte zu einer Verringerung der Fettmasse (FM) und einer Zunahme der mageren Körpermasse (LBM). Dies deutet darauf hin, dass Wachstumshormon einen wichtigen regulatorischen Einfluss auf die Körperzusammensetzung hat. HGH176-191 kann ebenfalls beteiligt sein, indem es die Stoffwechselprozesse von Adipozyten und Muskelzellen beeinflusst, die die Fettspeicherung und den Katabolismus sowie die Muskelsynthese und -wachstum regulieren. Zum Beispiel kann es die Lipolyse in Fettzellen fördern, um die Fettansammlung zu reduzieren, während es die Aufnahme von Aminosäuren und die Proteinsynthese in den Muskelzellen anregt, um die Muskelmasse zu erhöhen. Mit langfristigen Effekten hilft es, die Körperzusammensetzung zu verbessern und den Stoffwechsel zu steigern [3].
Energiestoffwechsel: Orexigene Nerven sind am Energiestoffwechsel des Körpers beteiligt, indem sie eine Vielzahl physiologischer Aktivitäten regulieren, unter anderem durch Blutzucker, Hungerhormon und Leptin. HGH176-191 kann mit diesen Regulatoren interagieren, um die Homöostase des Energiestoffwechsels zu beeinflussen. Wenn der Blutzucker gesenkt ist oder das Hungerhormon erhöht ist, fördert eine erhöhte Erregbarkeit der orexigenen Neuronen die Erregung, autonome Aktivität und die Motivation zum Konsumieren während der Vorbereitung auf die Nahrungsaufnahme und Verdauung. HGH176-191 kann die Energieaufnahme und -nutzung beeinflussen, indem es die Sekretion oder Signalübertragung verwandter Hormone in diesem Prozess reguliert. Zum Beispiel kann es die Leptin-Signalübertragung zum Hypothalamus beeinflussen, wodurch die Wahrnehmung des Energiestatus im Körper verändert und somit der Energiestoffwechsel angepasst wird. Langfristig ist dieser regulatorische Effekt entscheidend für die Aufrechterhaltung des Energiegleichgewichts des Körpers, und wenn diese Regulierung unausgewogen ist, kann dies zu viel oder zu wenig Energie aufnehmen und Probleme wie Fettleibigkeit oder Mangelernährung auslösen.
Auswirkungen auf tumorbedingten Stoffwechsel
In Studien zur Antikrebstherapie wurde festgestellt, dass Chitosan-Nanopartikel, die mit dem HGH176-191-Peptid in Kombination mit dem klinischen Chemotherapeuten Adriamycin geladen sind, eine stärkere antiproliferative Aktivität ³¹ gegen Brustkrebszelllinien (MCF-7) aufweisen als Chitosan-Nanopartikel, die allein mit Adriamycin geladen sind. Dies deutet darauf hin, dass HGH176-191 den Stoffwechsel von Tumorzellen beeinflussen und die krebshemmende Wirkung von Chemotherapeutika verstärken kann. Tumorzellen besitzen einzigartige metabolische Eigenschaften, wie eine verbesserte Glykolyse usw. HGH176-191 kann Tumorzellen empfindlicher auf Chemotherapeutika machen, indem es ihre Stoffwechselwege stört, etwa durch Beeinträchtigung der Aufnahme und Nutzung von Glukose, oder durch Veränderungen der Signalwege innerhalb der Tumorzellen. Eine langfristige Anwendung dieser Kombinationstherapie kann das Tumorwachstum effektiv hemmen, klinische Nebenwirkungen durch nicht gezielte Gewebeexposition reduzieren, die metabolische Homöostase der Tumorpatienten positiv beeinflussen und deren Lebensqualität sowie Überlebensqualität verbessern [4].
HGH176-191 Anti-Aging-Mechanismen
Zellreparatur und -regeneration
Die Anhäufung von Zellschäden und Alterung ist eine wichtige Grundlage für das Altern des Organismus. HGH176-191 kann die zelluläre Reparatur und Regeneration fördern, indem es die relevanten Signalwege innerhalb der Zellen aktiviert. Zum Beispiel kann es die Proliferation von Fibroblasten anregen und die zelluläre Aktivität steigern. Fibroblasten sind die wichtigsten Bestandteile der Haut, des Bindegewebes und anderer wichtiger Strukturen. Im Alterungsprozess der Haut führt der Rückgang der Fibroblastenfunktion zur Verringerung der Kollagen- und Elastinfasersynthese, und die Haut zeigt Falten, Schlaffe usw. HGH176-191 kann die Fähigkeit der Fibroblasten verbessern, diese extrazellulären Matrixkomponenten zu synthetisieren, sodass die Haut Elastizität und Festigkeit wiederherstellt und den Alterungsprozess der Haut auf mikroskopischer Ebene verlangsamt [5].
In molekularen Mechanismen könnte HGH176-191 den PI3K/AKT-Signalweg aktivieren. Dieser Signalweg spielt eine zentrale Rolle beim Zellwachstum, der Proliferation und dem Überleben. Wenn HGH176-191 an den entsprechenden Rezeptor auf der Zelloberfläche bindet, kann dies die Dimerisierung und Phosphorylierung des Rezeptors auslösen und dann das nachgeschaltete PI3K aktivieren, das AKT weiter phosphoryliert, und das aktivierte AKT kann durch eine Reihe von Kaskadenreaktionen die Expression zellzyklusbezogener Proteine fördern, die Proliferation und Reparatur der Zellen beschleunigen und widerstehen dem durch das Altern verursachten Zellfunktionsverschlechterung.
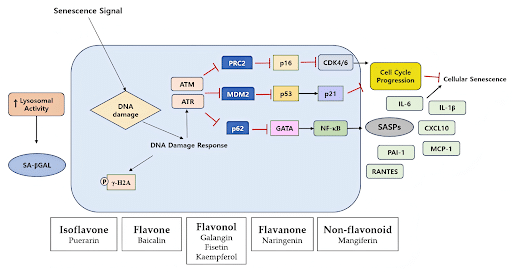
Abb. 1. Diagramm des Senezenz-Signalwegs und Polyphenole in gealterten dermalen Fibroblasten.
Quelle: MDPI [5]
Regulierung des Stoffwechselgleichgewichts
Mit zunehmendem Alter leiden Menschen häufig an Stoffwechselstörungen, wie Anomalien im Glukose- und Lipidstoffwechsel usw. HGH176-191 kann eine positive Rolle bei der Regulierung des Stoffwechselgleichgewichts spielen. Im Hinblick auf den Glukosestoffwechsel kann HGH176-191 den Insulinsignalweg beeinflussen, um die zelluläre Insulinsensitivität zu erhöhen, die Glukoseaufnahme und -nutzung zu fördern und eine Reihe altersbedingter Komplikationen wie Diabetes sowie daraus resultierende vaskuläre und neurologische Schäden durch erhöhten Blutzucker zu verhindern. Im Hinblick auf den Lipidstoffwechsel kann HGH176-191 die Katabolisierung von Adipozyten fördern, die übermäßige Fettansammlung im Körper verringern und das Risiko für Arteriosklerose und andere durch hohe Blutfette ausgelöste Herz-Kreislauf-Erkrankungen verringern, die eng mit dem Altern zusammenhängen [6].
Konkret kann HGH176-191 die Differenzierung und den Stoffwechsel von Adipozyten beeinflussen, indem es wichtige Transkriptionsfaktoren in Adipozyten reguliert, wie PPAR-γ, das ein wichtiger Regulator der Differenzierung und des Lipidstoffwechsels der Adipozyten ist, und HGH176-191 kann die Produktion der Adipozyten reduzieren, indem es die Aktivität von PPAR-γ hemmt und bestehende Adipozyten anregen. Durch Hemmung der PPAR-γ-Aktivität kann HGH176-191 die Produktion von Adipozyten reduzieren und die Liphylyse vorhandener Adipozyten fördern, Dadurch wird der Körperfettgehalt gesenkt, der Lipidstoffwechsel verbessert und die Stoffwechselstörungen im Laufe des Alters indirekt entgegengewirkt [7].
Antioxidativer Stress
Oxidativer Stress ist einer der wichtigsten Faktoren, die zur zellulären Alterung und zur Alterung des Organismus führen. Unter normalen Bedingungen sind die intrazellulären oxidativen und antioxidativen Systeme im Gleichgewicht, doch mit dem Alter steigt das oxidative Stressniveau, wodurch große Mengen freier Radikale wie reaktive Sauerstoffspezies (ROS) und reaktive Stickstoffspezies (RNS) entstehen, die intrazelluläre Biomoleküle wie DNA, Proteine und Lipide angreifen und so Schäden an Zellstruktur und Funktion verursachen. HGH176-191 könnte die Entwicklung von oxidativem Stress im zellulären System verhindern, indem es die Aktivität des intrazellulären antioxidativen Enzymsystems gegen oxidativen Stress erhöht. Studien haben gezeigt, dass es die Expression von antioxidativen Enzymen wie Superoxiddismutase (SOD) und Glutathionperoxidase (GPx) hochregulieren kann, die in der Lage sind, freie Radikale rechtzeitig aus Zellen zu entfernen, um oxidative Schäden zu reduzieren, normale zelluläre Funktion und Struktur aufrechtzuerhalten und das zelluläre Altern zu verzögern.
Im Hinblick auf die Genexpressionsregulation kann HGH176-191 auf die Promotorregion von Antioxidantienenzymgenen wirken und die Transkription und Translation dieser Enzymgene fördern, indem es an verwandte Transkriptionsfaktoren bindet, wodurch der Gehalt an antioxidativen Enzymen in der Zelle erhöht, die antioxidative Kapazität der Zelle verbessert und die durch oxidativen Stress verursachten Schäden an der Zelle abmildert werden was helfen kann, den Alterungsprozess des Organismus ganzheitlich zu verlangsamen [8].
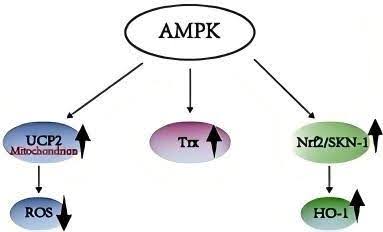
Abb. 2. Mechanismus der Anti-Aging-Wirkung von AMPK. AMPK begrenzt die ROS-Produktion, indem es die mitochondriale UCP2-Expression erhöht; Die Aktivierung von AMPK induziert die Trx-Expression; und AMPK aktiviert den Nrf2/SKN-1-Signalweg und induziert die Expression des Antioxidativen Häm-Oxygenase-1-Gens über den Nrf2-Signalweg.
Quelle: ELSEVIER [8]
Regulation der Immunfunktion
Der Rückgang der Funktion des Immunsystems ist eine der offensichtlichen Manifestationen des Alterns, was sich in der Verringerung der Anzahl der Immunzellen und der Abnahme der Immunaktivität widerspiegelt, was den Körper weniger widerstandsfähig gegen Krankheitserreger macht und anfällig für verschiedene Infektionskrankheiten und Tumore usw. macht. HGH176-191 könnte eine regulierende Wirkung auf das Immunsystem haben, und es kann die Immunfunktion des Organismus verbessern. Sie kann die Vermehrung und Differenzierung von Immunzellen wie T-Lymphozyten und B-Lymphozyten fördern, die Aktivität von Immunzellen verbessern und die Immunantwortfähigkeit des Körpers verbessern. Beispielsweise kann HGH176-191 während der Differenzierung von T-Lymphozyten die Sekretion von Zytokinen wie Interleukin-2 (IL-2) usw. regulieren, um die Differenzierung von T-Lymphozyten zu Effektor-T-Zellen mit immunologischer Aktivität zu fördern und die Fähigkeit des Körpers zu verbessern, Krankheitserreger abzutöten und zu schädigen.
Obwohl HGH176 - 191 nur ein kleiner Fragment von hGH ist, zeigt es wichtigen Forschungswert und potenzielle Anwendungsmöglichkeiten in den Bereichen Glukosestoffwechselregulation und Krebstherapie. Mit der Vertiefung der Forschung wird erwartet, dass sie neue Durchbrüche in der Behandlung verwandter Krankheiten bringt.
Artikelautor
Die oben genannte Literatur wurde von Dr. Velira Nyssén recherchiert, redigiert und organisiert.
Autor wissenschaftlicher Zeitschrift
Dr. P. E. Breukhoven ist assoziierter Forscher am Erasmus MC - Sophia Kinderkrankenhaus und der Abteilung für Allgemeinpädiatrie innerhalb von Erasmus MC mit Sitz in Rotterdam, Niederlande. Mit einer soliden akademischen Grundlage ist Dr. Breukhoven zudem mit der Erasmus-Universität Rotterdam verbunden und trägt zu interdisziplinären Forschungsbemühungen in der Region bei.
Mit Spezialisierung auf eine Vielzahl wissenschaftlicher Bereiche konzentriert sich ihre Forschung auf Endokrinologie und Stoffwechsel, Pädiatrie, Neurowissenschaften und Neurologie, öffentliche/umweltbezogene/arbeitsbezogene Gesundheit sowie Reproduktionsbiologie. Diese breite Expertise ermöglicht es Dr. Breukhoven, komplexe Gesundheitsherausforderungen in der Lebensspannenentwicklung und der Bevölkerungsgesundheit anzugehen und klinische Erkenntnisse mit translationalen Forschungsansätzen zu integrieren.
Als Teil der akademischen Gemeinschaft am Erasmus MC – einem führenden medizinischen Forschungsinstitut – spiegelt Dr. Breukhovens Arbeit ein Engagement für die Weiterentwicklung des Wissens in Kindergesundheit, neurologischen Erkrankungen und Umweltgesundheitsauswirkungen wider und fördert Kooperationen über institutionelle und disziplinäre Grenzen hinweg.
Zitate Quellenangaben
[1]. Khan SA, Ram N, Masood MQ. Muster des abnormen Glukosestoffwechsels bei Akromegalie und Einfluss der Behandlungsmethoden auf den Glukosestoffwechsel. CUREUS J MEDIZINISCHE WISSENSCHAFT. [Fachartikel]. 2021 2021-03-12; 13(3):e13852.10.7759/cureus.13852
[2]. Kappelgaard A, Kiyomi F, Horikawa R, Yokoya S, Tanaka T. Die Auswirkungen einer langfristigen Wachstumshormonbehandlung auf die metabolischen Parameter bei japanischen Patienten mit geringer Körpergröße, die klein für das Schwangerschaftsalter geboren wurden. HORM RES PAEDIAT. [Fachartikel; Multicenter-Studie; Randomisierte kontrollierte Studie]. 2014 2014-01-20; 81(4):272-9.10.1159/000358196
[3]. Breukhoven PE, Kerkhof GF, van Dijk M, Hokken-Koelega ACS. Langfristige Auswirkungen der GH-Behandlung in der Kindheit auf Körperzusammensetzung und Fettverteilung bei jungen Erwachsenen, die SGA geboren wurden. J CLIN ENDOCR METAB. [Fachartikel; Forschungsunterstützung, Nicht-US-amerikanische Gov't]. 2011 2011-12-01; 96(12):3710-6.10.1210/jc.2011-1658
[4]. Habibullah MM, Mohan S, Syed NK, Makeen HA, Jamal QMS, Alothaid H, Bantun F, Alhazmi A, Hakamy A, Kaabi YA, Samlan G, Lohani M, Thangavel N, Al-Kasim MA. Das humane Wachstumshormonfragment 176-191-Peptid erhöht die Toxizität von doxorubicinhaltigen Chitosan-Nanopartikeln gegen MCF-7-Brustkrebszellen. Drug Des Devel Ther. [Fachartikel]. 2022 2022-01-20; 16:1963-74.10.2147/DDDT. S367586
[5]. Lee JH, Park J, Shin DW. Der molekulare Mechanismus von Polyphenolen mit Anti-Aging-Aktivität in gealterten menschlichen dermalen Fibroblasten. MOLEKÜLE. [Fachartikel; Rezension]. 2022 2022-07-07; 27(14).10.3390/moleküle27144351
[6]. Bjørklund G, Shanaida M, Lysiuk R, Butnariu M, Peana M, Sarac I, Strus O, Smetanina K, Chirum Bolo S. Natural Compounds und Produkte aus einer Anti-Aging-Perspektive. MOLEKÜLE. [Fachartikel; Rezension]. 2022 2022-10-20; 27(20).10.3390/molecules27207084
[7]. Cavallini G, Donati A, Gori Z, Bergamini E. Auf dem Weg zum Verständnis des Anti-Aging-Mechanismusm Kalorienrestriktion. Curr Aging Sci. [Fachartikel]. 2008 2008-03-01; 1(1):4-9.10.2174/1874609810801010004
[8]. Zhang Y, Li Q, Niu Y, Wei K, Wang X, Niu B, Zhang L. Forschung zum Alterungsmechanismus und zu Medikamenten sowie zur Rolle von Stammzellen im Anti-Aging-Prozess. ERFAHRUNG: GERONTOL. [Fachartikel; Forschungsunterstützung, Nicht-US-amerikanische Regierung; Rezension]. 2023 2023-08-01; 179:112248.10.1016/j.exger.2023.112248
ALLE ARTIKEL UND PRODUKTINFORMATIONEN AUF DIESER WEBSITE DIENEN AUSSCHLIESSLICH ALS REFERENZ UND ZU BILDUNGSZWECKEN.
Die angebotenen Produkte sind streng für die In-vitro-Forschung vorgesehen (vom Latein: "in Glas"), was sich auf Studien außerhalb lebender Organismen bezieht. Diese Substanzen stellen keine pharmazeutischen Medikamente dar und wurden nicht von der US-amerikanischen Food and Drug Administration (FDA) zur Prävention, Behandlung oder Heilung von medizinischen Erkrankungen, Krankheiten oder Störungen geprüft oder zugelassen. Nach gesetzlichen Bestimmungen ist jegliche Einführung dieser Produkte in menschliche oder tierische biologische Systeme, unabhängig von der Verabreichungsmethode, ausdrücklich verboten.