Prostamax ist ein männliches Prostatagesundheitsergänzungsmittel, das auf Sägepalmenextrakt als Kernwirkstoff basiert und aus einer Einzeldosis von 320 mg standardisiertem Sägepalmen-Fruchtextrakt (Serenoa repens) besteht. Aus verfügbaren Studien geht hervor, dass sie modulatorische Effekte auf spezifische physiologische und pathologische Zustände zeigt, insbesondere bei der Behandlung der chronischen aseptischen Prostatitis und deren Auswirkungen auf die Chromatinstruktur von Lymphozyten. Das Produkt wird nach seiner Einführung in Hongkong im Jahr 2019 schnell zu einer wichtigen Option in der Prostataversorgung im asiatisch-pazifischen Raum.
Was ist Prostamax ?
Prostamax gehört zur Klasse von Peptid-Bioregulatoren, die physiologische Prozesse in Organismen modulieren. Sie beeinflusst die zelluläre Funktion und den Stoffwechsel, indem sie mit bestimmten Zielen innerhalb oder auf der Zelloberfläche interagiert und so den gesamten physiologischen Zustand beeinflusst.
Prostamax-Struktur
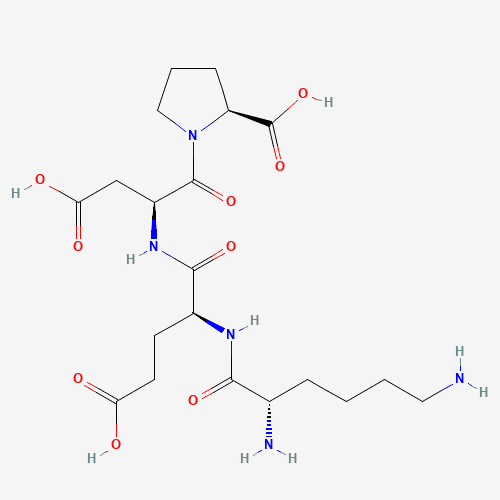
Prostamax-Forschung
Prostamax bei der Behandlung steriler chronischer Prostatitis
Bei chronischer, steriler Prostatitis wirkt Prostamax hauptsächlich, indem es die Symptome einer chronischen Entzündung lindert. Es verringert das Ausmaß chronischer Entzündungen, wie zum Beispiel durch die Verringerung von Symptomen wie Schwellungen, vaskulärer Verstopfung und lymphozytärer Infiltration. Außerdem verhindert es die Entwicklung von sklerotischen und atrophischen Prozessen. In Tierversuchen wurde beobachtet, dass es die sexuelle Aktivität bei Tieren steigert. Aus zellulärer und molekularer Sicht wird vermutet, dass es auf zelluläre Signalwege im Prostatagewebe wirken könnte, um die Expression und Freisetzung entzündungsbedingter Faktoren zu regulieren. Zum Beispiel die Hemmung der Produktion bestimmter proinflammatorischer Zytokine oder die Förderung der Sekretion entzündungshemmender Faktoren, wodurch die Entzündungsreaktion reduziert wird [1].
Linderung der entzündlichen Reaktion: Borovskaja-TG-Studien haben gezeigt, dass Prostamax die Schwere chronischer Entzündungen verringert, wie etwa Schwellungen, Gefäßverstopfung und lymphozytäre Infiltration. Der Wirkmechanismus könnte mit der Regulation der Expression entzündlicher Zytokine zusammenhängen. Während der Entzündung werden eine Reihe von Zytokinen wie Tumornekrosefaktor-α (TNF-α) und Interleukin-1-β (IL-1 β) in großen Mengen freigesetzt, was eine entzündliche Kaskade auslöst, und Prostamax kann die Entzündung lindern und Rötung, Schwellung und Infiltration von Prostatageweben reduzieren, indem entweder die proinflammatorische Zytokinproduktion hemmt oder die Expression entzündungshemmender Zytokine wie Interleukin-10 (IL-10) hochreguliert wird (Borovskaya et al., 2009). Symptome [1].
Während der Entwicklung der chronischen aseptischen Prostatitis können pathologische Veränderungen wie Sklerose und Atrophie des Prostatagewebes auftreten, was die normale Funktion der Prostata ernsthaft beeinträchtigen kann. Prostatan ist wirksam bei der Verhinderung der Entwicklung dieser pathologischen Prozesse. Der Mechanismus könnte mit der Regulation des extrazellulären Matrix-(ECM)-Stoffwechsels zusammenhängen. Bei Entzündungen geraten die Synthese und der Abbau der ECM aus dem Gleichgewicht, was zu einer übermäßigen Ablagerung von faserigem Gewebe und letztlich zur Gewebesklerose führt. Prostamax fördert die Aktivität von ECM-abbauenden Enzymen wie Matrix-Metalloproteinasen (MMPs) und hemmt gleichzeitig die Expression von Faktoren, die mit der ECM-Synthese verbunden sind, und erhält das Gleichgewicht der ECM, wodurch Sklerose und Atrophie des Prostatagewebes verhindert werden [2].
Verbesserung der sexuellen Funktion bei Tieren: Die Studie von Borovskaya TG ergab außerdem, dass Prostamax die sexuelle Funktion bei Tieren verbessert. Prostatitis wirkt sich oft negativ auf die sexuelle Funktion der Patienten aus, und die Wirkung von Prostamax eröffnet neue Möglichkeiten, ihre Lebensqualität zu verbessern. Der Mechanismus, durch den es die sexuelle Funktion verbessert, könnte mit der Regulation von Neurotransmittern und Hormonspiegeln zusammenhängen. So kann es beispielsweise die Freisetzung von Stickstoffmonoxid (NO) beeinflussen, einem wichtigen Signalmolekül in der penisen Erektion, process.NO die erektile Funktion verbessern kann, indem es die kavernöse glatte Muskelentspannung fördert und den Blutfluss zum Corpus cavernosum erhöht. Darüber hinaus kann Prostamax den Stoffwechsel oder die Signalübertragung von Sexualhormonen wie Androgenen beeinflussen und indirekt die sexuelle Funktion verbessern [2].
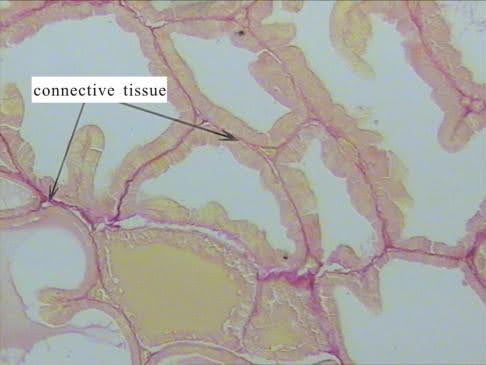
Abb. 1. Nebenanteil der Prostataratten mit chronischer Prostatitis abakteriell und erhalten Prostamaks. Die Menge an Kollagenfasern im Vergleich zur Kontrolle zu reduzieren. Picrofuchsin färben. ×200.
Quelle: PubMed [2]
Prostamax in der Immunmodulation
Bei Autoimmunerkrankungen greift das Immunsystem fälschlicherweise sein eigenes Gewebe an, was mit einer aberranten Aktivierung von Lymphozyten zusammenhängen könnte. Prostamax hat eine regulatorische Wirkung auf die Chromatinstruktur von Lymphozyten und beeinflusst die Aktivierungssignalwege von Lymphozyten, wodurch es eine Rolle bei Autoimmunerkrankungen spielt. Die DNA-Methylierung ist einer der wichtigen Regulatoren der Chromatinstruktur. In Lymphozyten ist die DNA-Methylierung an der Regulation der Expression lymphoidspezifischer Gene wie ITGAL (CD11a) und PRF1 (Perforin) beteiligt. Das DNA-Methylierungsmuster bestimmt die Zugänglichkeit von Chromatin, was wiederum die Bindung von Transkriptionsfaktoren an die DNA beeinflusst und somit die Genexpression reguliert [3].
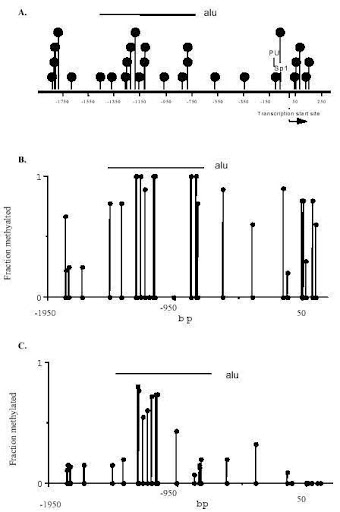
Abb. 2. ITGAL-Promotormethylierung. A. ITGAL-Promotorstruktur. Der ITGAL-Promoter wird angegeben, nummeriert relativ zum Transkriptionsstartort. Deoxycytosin-Reste in CG-Paaren werden durch die gefüllten Kreise dargestellt, die Transkriptionsstartstelle durch einen Pfeil und die PU.1- und Sp1-Bindungsstellen durch Linien. Die horizontale Linie zeigt einen Bereich mit Alu-Elementen an. B. ITGAL-Promotormethylierung in Fibroblasten. Die DNA wurde aus zwei Fibroblastenzelllinien isoliert, mit Bisulfit behandelt, dann wurde der ITGAL-Promotor in drei Regionen amplifiziert. Für jede verstärkte Region wurden 5 Fragmente geklont und sequenziert. Die gefüllten Kreise auf der X-Achse repräsentieren jeden potenziell methylierbaren dC-Rest, und die höher gefüllten Kreise stellen die durchschnittliche Methylierung für jede Stelle der 5 sequenzierten Fragmente aus beiden Fibroblastlinien dar. Auch hier zeigt die horizontale Linie eine Region mit Alu-Elementen an. C. ITGAL-Promotormethylierung in T-Zellen. T-Zell-DNA wurde ähnlich isoliert, mit Bisulfit behandelt, amplifiziert und sequenziert. Der Bereich von -1261 bis -68 entspricht der durchschnittlichen Methylierung von 5 Fragmenten von jedem der 6 Spender, während der Rest der Sequenz die durchschnittliche Methylierung von 5 Fragmenten von jedem der 4 normalen Spender darstellt. Auch hier zeigt die horizontale Linie eine Region mit Alu-Elementen an. Abgeändert gegenüber dem Original, veröffentlicht in Blood, 2002.
Quelle:PubMed [3]
Die Histonmodifikation ist ebenfalls ein wichtiger Weg, über den die Chromatinstruktur die Genexpression reguliert. Verschiedene Histonmodifikationen, wie Methylierung, Acetylierung und Phosphorylierung, können die Konformation und Zugänglichkeit des Chromatins verändern. So rekrutiert beispielsweise bei der Regulation des Lymphozyten-Antigenrezeptorlokus STAT5, aktiviert vom Interleukin-7-Rezeptor (IL-7R), transkriptionelle Kopplungen zum T-Zell-Antigenrezeptor (TCR) γ Locus, wodurch Histonmodifikationen induziert werden, die das Chromatin öffnen und Transkription sowie DNA-Rekombination fördern. Im Gegensatz dazu werden beim Abschalten der TCR-γ-Stelle hohe Mengen an Histon-H3-Lys9-Methylierung beobachtet, was die Genexpression hemmt.
Meski T zeigte, dass Chromatin aus menschlichen Lymphozyten bei bestimmten Temperaturen zwei Denaturierungsschritte durchläuft (tdvi = 94,4°C, qdvi = 50,8 J/g DNA; TdVIII = 105,1°C, QdVIII = 44,9 J/g DNA). Prostamax kann eine Wärmeumverteilung verursachen und die beiden Absorptions-Hotlines um 2,9 °C und 1,0 °C in niedrigere Temperaturen bewegen. Dies deutet darauf hin, dass Prostamax die thermische Stabilität des Chromatins beeinflusst und die Konformation des Chromatins verändern kann. Angenommen, die thermische Umverteilung zwischen Wärmeaufnahme VIII und VII ist mit der Relaxation von 30 nm groben Fasern zu 10 nm groben Fasern verbunden, impliziert dies, dass Prostamax die höhere Struktur des Chromatins beeinflussen kann, indem es vom engeren 30 nm Faserzustand in den relativ spärlichen 10 nm Faserzustand übergeht, was wiederum die Zugänglichkeit der Genexpression beeinträchtigt.
Prostamax-behandelte Lymphozyten hatten etwas niedrigere TdVII und TdVIII als unbehandelte Zellen, was mit subtilen strukturellen Veränderungen in der Organisation von 10- und 30-nm-dicken faserigen Nukleosomen assoziiert war. Nukleosomen sind die grundlegenden strukturellen Einheiten des Chromatins, und ihre Organisation und Anordnung beeinflussen die Kompaktheit des Chromatins und die Genzugänglichkeit. Daher kann Prostamax die Chromatinstruktur und letztlich die Genexpression beeinflussen, indem es die Organisation der Nukleosomen verändert [1].
Prostamax, als bioregulatorisches Peptid mit einem einzigartigen Wirkmechanismus und potenziellem Anwendungswert, zeigt bestimmte Forschungs- und Anwendungsmöglichkeiten bei der Behandlung chronischer aseptischer Prostatitis und immunbezogener Bereiche.
Artikelautor
Die oben genannte Literatur wurde von Dr. Velira Nyssén recherchiert, redigiert und organisiert.
Autor wissenschaftlicher Zeitschrift
Meskhi, Tamila, ist eine angesehene Forscherin, die mit dem G Eliava Institut für Bakteriophagen, Mikrobiologie und Virologie in Tiflis, Georgien, verbunden ist. Ihre Arbeit, die Teil des Labors für Gentechnik und Biotechnologie innerhalb des Instituts ist, erstreckt sich über eine Vielzahl wissenschaftlicher Disziplinen. Mit Spezialisierung auf Mikrobiologie, Biophysik sowie Biotechnologie und angewandte Mikrobiologie tragen Tamilas Forschungsprojekte maßgeblich zur Weiterentwicklung des Wissens in diesen wichtigen Bereichen bei. Da ihr Rekord algorithmisch generiert ist, unterstreicht dies die Bedeutung ihrer Arbeit, die wahrscheinlich verfolgt und für ihren potenziellen Einfluss auf die wissenschaftliche Gemeinschaft anerkannt wird.
Zitate Quellenangaben
[1]. Meskhu T, Khachidzr D, Barbakadze S, Madzhagaladze G, Gorgoshidze M, Monaselidze D, Lezhava T, Tadumadze N. Wirkung des Peptid-Bioregulators Prostamax auf das humane Lymphozyten-Heterochromatin in situ. Biophysik. 2004 0001-01-01; 49:978-80
[2]. Borovskaya TG, Pakhomova AV, Vychuzhanina AV, Poluektova ME, Fomina TI, Ermolaeva LA, Schemerova JA, Granstrem OK, Neplochov EA. Experimentelle Untersuchung der Wirksamkeit von Prostamax bei der Behandlung chronischer aseptischer Prostatitis und deren Komplikationen. Moderne Forschung zu Entzündungen. 2013; Bd.02No.03:5.10.4236/mri.2013.23007
[3]. Lu Q, Richardson B. Methoden zur Analyse der Rolle der DNA-Methylierung und der Chromatinstruktur bei der Regulation der Genexpression von T-Lymphozyten. BIOL WURDE ONLINE PROCEDIERT. [Fachartikel]. 2004 2004-01-20; 6:189-203.10.1251/bpo89
ALLE ARTIKEL UND PRODUKTINFORMATIONEN AUF DIESER WEBSITE DIENEN AUSSCHLIESSLICH ALS REFERENZ UND ZU BILDUNGSZWECKEN.
Die angebotenen Produkte sind streng für die In-vitro-Forschung vorgesehen (vom Latein: "in Glas"), was sich auf Studien außerhalb lebender Organismen bezieht. Diese Substanzen stellen keine pharmazeutischen Medikamente dar und wurden nicht von der US-amerikanischen Food and Drug Administration (FDA) zur Prävention, Behandlung oder Heilung von medizinischen Erkrankungen, Krankheiten oder Störungen geprüft oder zugelassen. Nach gesetzlichen Bestimmungen ist jegliche Einführung dieser Produkte in menschliche oder tierische biologische Systeme, unabhängig von der Verabreichungsmethode, ausdrücklich verboten.